TRANS-INDETERMINALIDADE GRACELI.
NÃO É POSSÍVEL DETERMINAR NEM A POSIÇÃO OU O MOMENTUM DE UMA PARTÍCULA, FENÔMENO, OU ENERGIA. EM UM MESMO TEMPO. OU EM DOIS TEMPOS DIFERENTES. E SENDO VARIÁVEL CONFORME O SDCTI GRACELI.
COM ISTO SE TEM UMA EXCLUSAÕ DE GRACELI PARA MOMENTUM E ESTADO QUÂNTICO [INDEPENDENTE DE SER DE FÉRMIONS OU NÃO].
E UM INCERTEZA GENERALIZADA.
O princípio de exclusão de Pauli pode ser deduzido a partir da hipótese de que um sistema de partículas só pode ocupar estados quânticos anti-simétricos. De acordo com o teorema spin-estatística, sistemas de partículas idênticas de spin inteiro ocupam estados simétricos, enquanto sistemas de partículas de spin semi-inteiro ocupam estados anti-simétricos; além disso, apenas valores de spin inteiros ou semi-inteiros são permitidos pelos princípio da mecânica quântica.
Como discutido no artigo sobre partículas idênticas, um estado anti-simétrico no qual uma das partículas está no estado (nota) enquanto a outra está no estado é
- X
- FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.x[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.+ FUNÇÃO DE RADIOATIVIDADE, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICAENERGIA DE PLANCKX
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
No entanto, se e são exatamente o mesmo estado, a expressão acima é identicamente nula:
Isto não representa um estado quântico válido, porque vetores de estado que representem estados quânticos têm obrigatoriamente que ser normalizáveis, isto é devem ter norma finita. Em outras palavras, nunca poderemos encontrar as partículas que formam o sistema ocupando um mesmo estado quântico.
Pode-se exprimir o princípio da incerteza nos seguintes termos:
O produto da incerteza associada ao valor de uma coordenada xi e a incerteza associada ao seu correspondente momento linear pi não pode ser inferior, em grandeza, à constante reduzida de Planck.[4] Em termos matemáticos, exprime-se assim:
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Um equilíbrio químico é a situação em que a proporção entre os reagentes e produtos de uma reação química se mantém constante ao longo do tempo. Foi estudado pela primeira vez pelo químico francês Claude Louis Berthollet em seu livro Essai de statique chimique de 1803.[1]
Teoricamente, toda a reação química ocorre nos dois sentidos: de reagentes se transformando em produtos e de produtos se transformando de volta em reagentes. Contudo, em certas reações, como a de combustão, praticamente 100% dos reagentes são convertidos em produtos, e não se observa ocorrer o contrário (ou pelo menos não em escala mensurável); tais reações são chamadas de irreversíveis. Há também uma série de reações nas quais logo que certa quantidade de produto(s) é formada, este(s) torna(m) a dar origem ao(s) reagente(s); essas reações possuem o nome de reversíveis. O conceito de equilíbrio químico restringe-se às reações reversíveis.
Apesar das concentrações do(s) reagente(s) e do(s) produto(s) serem constantes no equilíbrio químico de uma reação, os fenômenos direto e inverso do processo, que é reversível, continuam ocorrendo, ambos na mesma velocidade. Dessa forma, as reações direta e inversa se anulam, o que justifica o fato das concentrações do(s) produto(s) e do(s) reagente(s) serem constantes no equilíbrio químico, apesar da reação nunca ser interrompida.
Reversibilidade de reações químicas[editar | editar código-fonte]
Um exemplo de reação reversível é a da produção da amônia (NH3) a partir do gás hidrogênio (H2) e do gás nitrogênio (N2) — que faz parte do Processo de Haber:
Note-se que a seta dupla () significa que a reação ocorre nos dois sentidos, e que o subscrito (g) indica que a substância se encontra na fase gasosa.
Nesta reação, quando as moléculas de nitrogênio e as de hidrogênio colidem entre si, há uma certa chance da reação entre elas ocorrer, assim como quando moléculas de amônia colidem entre si há uma certa chance de elas se dissociarem e de se reorganizarem em H2 e N2.
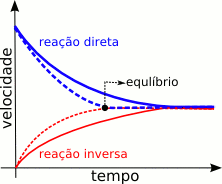
No início do processo, quando há apenas uma mistura de hidrogênio e nitrogênio, as chances das moléculas dos reagentes (H2 e N2) colidirem umas com as outras é a máxima de toda a reação, o que fará com que a taxa (ou velocidade) com que a reação ocorre também o seja. Porém à medida com que a reação se processa o número de moléculas de hidrogênio e de nitrogênio diminui, reduzindo dessa forma as chances de elas colidirem entre si e, consequentemente, a velocidade desse sentido da reação. Por outro lado, com o avançar da reação, o número de moléculas de amônia vai aumentando, o que faz com que cresçam as chances de elas colidirem e de se voltar a formar hidrogênio e nitrogênio, elevando assim a velocidade desse sentido da reação. Por fim chegará um momento em que tanto a velocidade de um dos sentidos quanto a do outro serão idênticas, nesse ponto nenhuma das velocidades variará mais (se forem mantidas as condições do sistema onde a reação se processa) e ter-se-á atingido o equilíbrio químico, conforme ilustrado nas figuras abaixo:
Um raciocínio similar, em princípio, pode ser aplicado para qualquer equilíbrio.
Deve-se salientar que quando uma reação atinge o equilíbrio ela não para. Ela continua se processando, porém tanto a reação direta como a inversa ocorrem à mesma velocidade, e desse jeito a proporção entre os reagentes e os produtos não varia . Por outras palavras, estamos na presença de um equilíbrio dinâmico (e não de um equilíbrio estático).
Constante de equilíbrio[editar | editar código-fonte]
"Por exemplo, a constante dessa reação na temperatura de 1000 K é 0,0413, note que a constante é ADIMENSIONAL*."
- Referência: Atkins, Peter e Jones, Loretta - Princípios de Química 3º Edição
- O equilíbrio químico é atingido quando, na mistura reacional, as velocidades das reações direta (reagentes formando produtos) e inversa (produtos formando regenerando os reagentes) ficam iguais.
Uma vez atingido o equilíbrio a proporção entre os reagentes e os produtos não é necessariamente de 1:1 (lê-se um para um). Essa proporção é descrita por meio de uma relação matemática, mostrada a seguir:
Dada a reação genérica:
onde A, B, Y e Z representam as espécies químicas envolvidas e a, b, y e z os seus respectivos coeficientes estequiométricos. A fórmula que descreve a proporção no equilíbrio entre as espécies envolvidas é:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Os colchetes representam o valor da concentração (normalmente em mol/L) da espécie que está simbolizada dentro dele ([A] = concentração da espécie A, e assim por diante). é uma grandeza chamada de constante de equilíbrio da reação. Cada reação de equilíbrio possui a sua constante, a qual sempre possui o mesmo valor para uma mesma temperatura. De um modo geral, a constante de equilíbrio de uma reação qualquer é calculada dividindo-se a multiplicação das concentrações dos produtos (cada uma elevada ao seu respectivo coeficiente estequiométrico) pela multiplicação das concentrações dos reagentes (cada uma elevada ao seu relativo coeficiente estequiométrico).
Um exemplo disso é a formação do trióxido de enxofre (SO3) a partir do gás oxigênio (O2) e do dióxido de enxofre (SO2(g)) — uma etapa do processo de fabricação do ácido sulfúrico:
A constante de equilíbrio desta reação é dada por:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
É possível determinar experimentalmente o valor da constante de equilíbrio para uma dada temperatura. Por exemplo, a constante dessa reação na temperatura de 1000 K é 0,0413. A partir dela, dada uma certa quantidade conhecida de produtos adicionados inicialmente em um sistema nessa temperatura, é possível calcular por meio da fórmula da constante qual será a concentração de todas as substâncias quando o equilíbrio for atingido. É importante notar que, Kc para uma equação química SÓ depende da temperatura, não é alterado por catalisador e mede a espontaneidade da reação direta, a partir da condição padrão ( 1 mol/l ou 1 atm )
Utilizando a relação:
- , onde ΔG é a energia livre de Gibbs, T a temperatura absoluta e ΔS e a variação da entropia.
Podemos colocá-la da seguinte forma:
- (I) ( É possível por ser função de estado )
E sabendo que:
- (II) , onde U e a energia interna, P é a pressão e V o volume.
Derivando (I) temos:
- (III),
Sabendo que:
- (IV)
- x
- FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.x[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.+ FUNÇÃO DE RADIOATIVIDADE, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICAENERGIA DE PLANCKX
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Tendo que:
- (V)
Inserindo (IV) e (V) em (III)
- , onde TdS = 0 pois,
Para P e T constantes temos:
- , onde PdV = 0
Integrando a equação de Gº ( G padrão ) a G e de Pº ( "P zero" = P padrão ) temos :
- , onde n é o nº de moles, R a constante universal dos gases.
- x
- FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.x[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.+ FUNÇÃO DE RADIOATIVIDADE, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICAENERGIA DE PLANCKX
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Onde Pº = 1 atm, note que daqui fica extremamente claro que o K é adimensional, pois P/Pº é adimensional.
Chegamos:
- (VI) , onde ln P é o logaritmo de base e de P.
Agora tendo uma reação:
aA + bB cC + dD (reação direta)
cC + dD aA + bB (reação inversa)
, onde Gp é a energia dos produtos e Gr a energia dos reagentes.
Colocando (VI) nessa equação, conclui - se:
Onde X = A multiplicação das pressões parciais dos produtos elevado a seus respectivos coeficientes estequiométricos e Y idem para os reagentes.
- , onde Q é o quociente da reação.
Para o equilíbrio temos que K = Q e ΔG = 0*
- ΔG = 0 pois a reação direta e inversa não são espontâneas, portanto é possível afirmar que o equilíbrio foi atingido!
Temos por fim:
- , concluindo:
- x
- FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.x[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.+ FUNÇÃO DE RADIOATIVIDADE, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICAENERGIA DE PLANCKX
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Note que aqui fica mais claro ainda que o K é adimensional e que o K de uma reação elementar é o mesmo, caso a reação não seja elementar, por causa da função de estado, onde ΔGf = ΔGi, logo K não depende do caminho percorrido, só dependendo a temperatura. Note também que K mede a espontaneidade a partir da condição padrão.
As leis de Guldberg-Waage e de Arrhenius[editar | editar código-fonte]
É possível relacionar a lei de Guldberg-Waage e a Lei de Arrhenius a essa última fórmula. Assim, pela Lei de Guldberg-Waage:
Onde k1,2 são as constantes cinéticas das reações direta e inversa, respectivamente, bem como [X1] e [X2] são as concentrações dos reagentes
Logo, no equilíbrio, v1 = v2, onde v1 é Velocidade da reação direta e v2 da inversa:
E para Lei de Arrhenius temos:
- x
- FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.x[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.+ FUNÇÃO DE RADIOATIVIDADE, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICAENERGIA DE PLANCKX
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Onde:
H é a entalpia, S é a entropia e Eap,r são as energias de ativação dos produtos e dos reagentes respectivamente. Dessa forma:
Constante para a soma de reações[editar | editar código-fonte]
Se uma reação química pode ser expressa pela soma de duas ou mais reações (ou etapas individuais), então a constante de equilíbrio da reação global será a multiplicação das constantes de cada uma das reações individuais.
| 2P(g) + 3Cl2(g) 2PCl3(g) | |
| PCl3(g) + Cl2(g) PCl5(g) | |
| 2P(g) + 5Cl2(g) 2PCl5(g) |
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Neste caso, a terceira reação é igual à soma da primeira mais duas vezes a segunda:
| + | 2P(g) + 3Cl2(g) 2PCl3(g) |
| PCl3(g) + Cl2(g) PCl5(g) | |
| PCl3(g) + Cl2(g) PCl5(g) | |
| 2P(g) + 5Cl2(g) 2PCl5(g) |
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
E a sua constante de equilíbrio pode ser expressa por:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Pode se perceber que caso uma reação apareça duas ou mais vezes na soma, ela aparece esse mesmo número de vezes na multiplicação.
Relação entre a velocidade da reação e a constante de equilíbrio[editar | editar código-fonte]
Conforme já mencionado, no equilíbrio a velocidade tanto da reação inversa quanto a da direta são iguais. Por sua vez, a velocidade de uma reação depende de uma outra constante chamada de constante de velocidade (simbolizada aqui por ); e é possível encontrar uma relação entre as constantes de velocidade das reações direta e indireta, e a constante de equilíbrio.
Para demonstrar isso, considere-se o seguinte equilíbrio genérico (supondo que as suas reações ocorram cada qual em uma única etapa):
| 2A X + Y |
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Agora vejamos as duas reações que ocorrem nele, juntamente com a expressão de suas respectivas velocidades ():
| 2A → X + Y | |
| X + Y → 2A |
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
É importante frisar que o expoente que eleva as concentrações das espécies na fórmula da velocidade não necessariamente é igual ao respectivo coeficiente estequiométrico da espécie na reação, contudo o expoente certamente será assim se a reação se processar em uma única etapa (conforme se está considerando nessa situação).
Uma vez que as velocidades de ambas as reações são idênticas no equilíbrio, pode-se igualá-las:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Rearranjando a equação, tem-se:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Observemos que a expressão do membro esquerdo é idêntica à fórmula do equilíbrio dessa reação. Então podemos escrever:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Esta relação é válida para qualquer equilíbrio cujas reações ocorram em uma única etapa, o que pode ser facilmente constatado por essa mesma dedução para outros equilíbrios.
No caso de as reações se processarem em mais de uma etapa, basta lembrar que a reação global nada mais é que a soma das reações de cada etapa. Para cada uma das etapas pode-se fazer essa mesma dedução, e então somar cada reação (o que significa multiplicar as suas constantes). Dessa forma teremos para uma reação de múltiplas etapas:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Sendo , , , e assim por diante as constantes de velocidades de cada etapa.
Equilíbrio heterogêneo[editar | editar código-fonte]
Quando todas as substâncias envolvidas no equilíbrio se encontram no mesmo estado físico diz-se que temos um equilíbrio homogêneo, que é o caso de todos os equilíbrios apresentados aqui até então. Analogamente, os equilíbrios onde estão envolvidas mais de uma fase são chamados de equilíbrios heterogêneos, como o seguinte:
Ni(s) + 4CO(g) Ni(CO)4(g)
Note-se que o subscrito (s) significa que a espécie se encontra no estado sólido. Equilíbrios heterogêneos, como este, frequentemente apresentam ao menos um sólido puro ou um líquido puro.
Na expressão da constante de equilíbrio temos as concentrações das espécies envolvidas. A concentração pode ser calculada dividindo-se o número de mols da substância pelo volume que ela ocupa. O número de mols representa a quantidade de matéria e, por isso, ele é proporcional a massa; assim o número de mols dividido pelo volume é proporcional à massa dividida pelo volume.
A densidade de algo é justamente calculada dividindo-se a sua massa pelo seu volume ocupado. No caso de uma substância pura, toda a sua massa corresponde à de uma única substância, e assim a sua "concentração" do seu número de mols dividido pelo volume é proporcional a sua densidade (massa dividida pelo volume).
A densidade de uma dada substância em dadas condições é uma propriedade intensiva, ou seja, é a mesma independentemente do quanto dessa substância houver. Dessa forma pode-se concluir que a concentração de um sólido ou um líquido puro (que são virtualmente incompressíveis) é a mesma independentemente de quanto houver deles (já um gás, que pode ser comprimido sem dificuldade, tem a sua concentração variada facilmente). Por essa razão se simplifica as expressões das constantes de equilíbrio omitindo-se a concentração de sólidos e líquidos puros.
Com isso, a expressão para a constante do último equilíbrio apresentado fica:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Equilíbrio gasoso[editar | editar código-fonte]
Pela equação dos gases perfeitos tem-se que para cada gás de uma mistura gasosa:
,
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
onde é a pressão parcial de um gás qualquer (ou seja, a pressão que ele teria caso estivesse apenas ele no recipiente), é o volume ocupado pela mistura, é o número de mols do gás, é a constante dos gases perfeitos, e a temperatura em kelvin.
Rearranjando a equação, teremos:
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
O membro esquerdo (/) é a fórmula para o cálculo da concentração molar do gás. A constante é sempre a mesma e a temperatura não varia em um sistema que permanece em equilíbrio químico, assim o único fator que pode variar na equação em um equilíbrio é a pressão parcial . Dessa forma pode-se dizer que a concentração do gás é proporcional à sua pressão parcial.
Com base nisso, também é possível escrever a fórmula da constante de equilíbrio usando-se as pressões parciais dos gases envolvidos, no lugar de suas concentrações. Por exemplo:
| H2(g) + I2(g) 2HI(g) |
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Observe-se que agora a constante de equilíbrio está representada por , em vez de (quando o cálculo foi feito usando-se as concentrações dos gases). Essas duas constantes para um mesmo caso possuem valores diferentes uma da outra, então é importante especificar qual das duas se está usando quando se está lidando com um equilíbrio.
Adição ou remoção de reagentes (Não serve para sólidos)[editar | editar código-fonte]
Ao se alterar a quantidade de uma substância, também se está mexendo na velocidade em que a reação se processa (pois se estará mudando as chances de as substâncias reagirem entre si). Dessa forma, a velocidade das reações direta e inversa deixa de ser igual: se uma substância foi retirada de uma das reações, essa passará a ser mais lenta; e, analogamente, ela passará a ser mais rápida se uma substância for adicionada a ela. Assim ocorre que se algo for acrescentado, o equilíbrio tende a reduzir a quantidade dessa substância e vice-versa. Para garantir que a reação se torne reversa
Tal resposta do equilíbrio pode ser sumarizada pelo assim chamado Princípio de Le Chatelier:
| Quando uma perturbação externa é aplicada a um sistema em equilíbrio dinâmico, o equilíbrio tende a se ajustar para diminuir o efeito da perturbação. |
À medida que as reações se processam, as suas velocidades vão se aproximando até que se igualem e assim é atingido novamente o equilíbrio. A constante do equilíbrio será a mesma da de antes de se adicionar ou remover substâncias.
Compressão[editar | editar código-fonte]
Um equilíbrio gasoso pode ser afetado pela compressão. De acordo com o princípio de Le Chatelier, com o aumento da pressão o equilíbrio tende a se deslocar no sentido de diminuir essa pressão, o que significa favorecer a reação que resulte no menor número de moléculas no estado gasoso. Nesse caso, a o valor da constante de equilíbrio também não é alterado.
Para se observar tal efeito, considere-se esse equilíbrio:
| N2O4(g) 2NO2(g) |
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
As concentrações podem ser escritas como o seu número de mols dividido pelo volume (), então teremos:
x
x
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Se o valor de (volume) diminuir, é preciso que o número de mols do N2O4 aumente para que o valor da constante de equilíbrio permaneça o mesmo. Na reação, esse reagente representava metade do número de moléculas do produto. O mesmo raciocínio pode ser aplicado em qualquer equilíbrio gasoso.
Temperatura[editar | editar código-fonte]
É encontrado experimentalmente que a formação de produtos de uma reação exotérmica (isto é, que liberta energia) é favorecida com a diminuição da temperatura, ao passo que a formação de produtos em uma reação endotérmica (isto é, que absorve energia) é favorecida com o aumento da temperatura.
Em um equilíbrio, se uma reação é endotérmica a outra necessariamente é exotérmica, e vice-versa. Aumentar ou diminuir a temperatura fará com que a velocidade de uma das reações aumente e a da outra diminua. As velocidades das reações se igualarão novamente depois de um tempo; porém nesse caso como temos o favorecimento e o desfavorecimento da formação de certas substâncias, a constante de equilíbrio nessa nova temperatura não será mais a mesma da temperatura anterior.
Catalisador[editar | editar código-fonte]
A adição de um catalisador direciona a reação para um novo mecanismo, o qual é mais rápido do que o sem a catálise. Contudo, o catalisador não afeta o valor da constante de equilíbrio, ele apenas faz com que o equilíbrio seja atingido em um tempo menor, conforme mostrado na figura a seguir:
Atenção: O equilíbrio não é deslocado com a presença do catalisador.
Relação entre as constantes Kp e Kc[editar | editar código-fonte]
Existe uma relação matemática entre as constantes de equilíbrio em função da concentração Kc e em função da pressão parcial Kp, baseada na equação de Clapeyron:
FUNÇÃO FUNDAMENTAL E GERAL DE GRACELI.
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia.x
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
em que: R é a constante universal dos gases, T é a temperatura absoluta e Δn é a diferença entre a soma dos coeficientes inteiros dos produtos gasosos e a soma dos coeficientes inteiros dos reagentes gasosos. Por exemplo, no equilíbrio:
Essa expressão matemática apresenta uma limitação, não admitindo a presença de um ou mais líquidos na reação em questão. Isso não significa que a reação não apresente Kp e Kc, significa apenas que a expressão é inválida para esse caso.



 [EQUAÇÃO DE DIRAC].
[EQUAÇÃO DE DIRAC].
 + FUNÇÃO DE RADIOATIVIDADE
+ FUNÇÃO DE RADIOATIVIDADE
 + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ FUNÇÃO DE TUNELAMENTO QUÂNTICO. + ENTROPIA REVERSÍVEL
+ ENTROPIA REVERSÍVEL ![\sigma =q(n\mu _{n}+p\mu _{p})[\Omega .cm]^{{-1}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/53d1173dd9d9ec55715f1f4beb1ea5dcd4932bc8) FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA ENERGIA DE PLANCK
ENERGIA DE PLANCK





![K_{c}={\frac {[{\mbox{Y}}]^{{\mbox{y}}}\cdot [{\mbox{Z}}]^{{\mbox{z}}}}{[{\mbox{A}}]^{{\mbox{a}}}\cdot [{\mbox{B}}]^{{\mbox{b}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec1a3ac295d3316425779601273c6641a5a4c18f)

![K_{c}={\frac {[{\mbox{SO}}_{{\mbox{3}}}]^{{\mbox{2}}}}{[{\mbox{SO}}_{{\mbox{2}}}]^{{\mbox{2}}}\cdot [{\mbox{O}}_{{\mbox{2}}}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7b91b2f2333ee8ba08b8b8946cdec820e7b51a51)













![{\displaystyle \Delta G=\Delta G^{0}+RT\ln[X/Y]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a0f441168e8fd76275d4573ccad4f3f8d5a5f97d)



![{\displaystyle v1=k1[X1],v2=k2[X2]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/adb632714fde07ba9936cb11713a290801891d5a)
![{\displaystyle k1[X1]=k2[X2]\Rightarrow k1/k2=[X2]/[X1]=K}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e1cfdfaf9915157271ebec94d5a5e2c70232ef7b)
![{\displaystyle K=e^{-\Delta G^{o}/RT}=e^{-(\Delta H^{o}-\Delta S^{o}T)/RT}=[e^{-Eap/RT}][e^{Sp/R}]/[e^{-Ear/RT}][e^{Sr/R}]=k1/k2}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1f2f6beb277a81c9776ac53423fa21e8f4b65b08)

![K'_{c}={\frac {[{\mbox{PCl}}_{{\mbox{3}}}]^{{\mbox{2}}}}{[{\mbox{P}}]^{{\mbox{2}}}\cdot [{\mbox{Cl}}_{{\mbox{2}}}]^{{\mbox{3}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d78020c2da916da17ef37294ac778a9b9dca4385)
![K''_{c}={\frac {[{\mbox{PCl}}_{{\mbox{5}}}]}{[{\mbox{PCl}}_{{\mbox{3}}}]\cdot [{\mbox{Cl}}_{{\mbox{2}}}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/40dc1930181c6472f2a7f8e570f463875ca804ef)
![K_{c}={\frac {[{\mbox{PCl}}_{{\mbox{5}}}]^{{\mbox{2}}}}{[{\mbox{P}}]^{{\mbox{2}}}\cdot [{\mbox{Cl}}_{{\mbox{2}}}]^{{\mbox{5}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6f5e7eace836ee4c7f6ad7c8bb5daf64f6c1446e)

![K_{c}={\frac {[{\mbox{PCl}}_{{\mbox{3}}}]^{{\mbox{2}}}}{[{\mbox{P}}]^{{\mbox{2}}}\cdot [{\mbox{Cl}}_{{\mbox{2}}}]^{{\mbox{3}}}}}\cdot {\frac {[{\mbox{PCl}}_{{\mbox{5}}}]}{[{\mbox{PCl}}_{{\mbox{3}}}]\cdot [{\mbox{Cl}}_{{\mbox{2}}}]}}\cdot {\frac {[{\mbox{PCl}}_{{\mbox{5}}}]}{[{\mbox{PCl}}_{{\mbox{3}}}]\cdot [{\mbox{Cl}}_{{\mbox{2}}}]}}={\frac {[{\mbox{PCl}}_{{\mbox{5}}}]^{{\mbox{2}}}}{[{\mbox{P}}]^{{\mbox{2}}}\cdot [{\mbox{Cl}}_{{\mbox{2}}}]^{{\mbox{5}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e4740b5ab47d7ec30b6eca0ed92d4c2ed81379ca)

![K_{c}={\frac {[{\mbox{X}}]\cdot [{\mbox{Y}}]}{[{\mbox{A}}]^{{\mbox{2}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/20ee8298ed7cbbca5e6599d3e479b91b66ff290e)

![r=k\cdot [{\mbox{A}}]^{{\mbox{2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/dcfa5f84d865f067917cb7faa9f73a948ec3044c)
![r'=k'\cdot [{\mbox{X}}]\cdot [{\mbox{Y}}]](https://wikimedia.org/api/rest_v1/media/math/render/svg/9a202ba1999397696f1bac82fc4edc7a0421dd63)
![k\cdot [{\mbox{A}}]^{{\mbox{2}}}=k'\cdot [{\mbox{X}}]\cdot [{\mbox{Y}}]](https://wikimedia.org/api/rest_v1/media/math/render/svg/7b32ef1a1c3044ee497e20229128e71d80dc1ae5)
![{\frac {[{\mbox{X}}]\cdot [{\mbox{Y}}]}{[{\mbox{A}}]^{{\mbox{2}}}}}={\frac {k}{k'}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cfe68aa26183e310f49a6389cd5348d4a63b7c72)






![K_{c}={\frac {[{\mbox{Ni}}{\mbox{(CO)}}_{4}]}{[{\mbox{CO}}]^{{\mbox{4}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0764e4904d7be4e37de7c265d4db46c4d68ac6d7)










![K_{c}={\frac {[{\mbox{NO}}_{{\mbox{2}}}]^{{\mbox{2}}}}{[{\mbox{N}}_{{\mbox{2}}}{\mbox{O}}_{{\mbox{4}}}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/255a4a323ce1d95c6aa18f28ea916328edbd0aa6)